
최근 경색된 국내 투자 상황을 극복하고 글로벌 사업화를 위한 연구개발 SEED 확보를 위해 바이오헬스분야 유망창업기업인 초격차 기업들이 대규모 글로벌 IR에 나섰다.
중소벤처기업부가 지원하는 초격차 스타트업 1000+ 프로젝트의 혁신분야창업패키지(신산업) 지원사업 바이오헬스분야 주관기관인 안전성평가연구소(소장 정은주)는 지난 16일 양재 L타워에서 바이오분야 전문 국내외 VC들이 참석한 가운데 ‘글로벌 IR데이'를 성료했다고 밝혔다.
한국보건산업진흥원과 안전성평가연구소 등이 공동 주최한 ‘글로벌 오픈이노베이션 위크’ 행사의 일환으로, 초격차 사업의 주관기관인 안전성평가연구소가 개최한 이번 행사에서는 바이오헬스분야 국내 투자유치 전문 기관 외에도 미국 및 유럽 현지 바이오 분야 전문 VC들이 대거 참여해 국내 바이오 유망스타트업들의 글로벌 투자 유치 가능성을 확인했다.
특히 이번행사는 최근 바이오분야 국내는 물론 전 세계적으로 바이오분야 투자 환경이 경색된 가운데 글로벌 임상 등 연구개발을 위한 시드(SEED) 확보를 위한 글로벌 투자유치의 촉진제가 될 것으로 기대되고 있다. 한편으로는 현지 전문가들의 의견과 평가를 바탕으로 글로벌 사업화의 전략적 접근과 방법을 모색하는 기회도 될 것으로 점쳐 진다.
이를 위해 프로엡텍, 일리아스바이오로직스, 넥스아이 등 총 12개 유망 바이오스타트업들이 이번 IR행사에 참여했으며, 대교인베스먼트 등의 국내 민간 투자기관과 보스톤 기반의 전문 VC, 유럽 내 현지 창업기업 대상 투자 전문 VC 등 총 9개 기관이 이번 IR행사에 참여했다. 또한 기업별 기술 발표(IR)외에도 사전 매칭을 통한 전문기관과의 투자 상담과 행사 참여 제약 등 유관 산업계 기업들과의 파트너링도 동시에 진행됐다.
안전성평가연구소는 “최근 국내 바이오 산업계 내에서 최대 현안은 연구개발 자금 확보를 위한 지속적인 투자유치”라며 “국내 바이오기업들의 글로벌 사업화 및 투자 유치 역량이 충분한 만큼 이번 행사가 국내 바이오 산업계 내에 글로벌 투자 유치의 불씨를 살리는, 작지만 의미있는 계기가 되길 바란다”고 말했다.
한편 안전성평가연구소는 한국보건산업진흥원과 한국제약바이오협와 공동으로 지난 14일부터 17일까지 양재동 L타워 등에서 국내 제약바이오 산업의 오픈이노베이션 활성화를 위한 ‘제약바이오 글로벌 오픈이노베이션 위크’를 개최했다.

희귀질환에 대한 기전 연구, 후보물질 발굴, 개발 동향 등 다양한 정보와 데이터를 공유하는 자리가 마련됐다.
희귀유전질환 심포지엄 조직위원회가 주최하는 제4회 희귀유전질환 심포지엄이 ‘Development of new drugs for Rare neuropathy’를 주제로 16일 부산 동래구 호텔 농심에서 개최됐다. 심포지엄은 17일까지 진행된다.
심포지엄의 주관을 맡은 부산대학교 차정인 총장은 환영사를 통해 “이번 심포지엄은 희귀질환 각 분야의 현장 경험과 기술적 지식이 풍부한 전문가들의 조력으로 성공적인 심포지엄이 될 것”이라며 “이번 심포지엄을 계기로 희귀 유전질환 분야 연구가 더욱 활성화되고 창업 등 산업 분야로 연계가 촉진되길 바란다”고 말했다.
이어 “무엇보다 희귀 유전질환으로 고통받고 있는 환자들과 가족들에게 새로운 희망을 제시할 수 있는 초석이 되길 기대한다”고 강조했다.
축사를 맡은 생화학분자생물학회 권호정 회장(연세대학교 생명공학과 교수)은 “희귀질환은 아직 환자 수는 그리 많지 않지만, 특정 유전자 질환으로 어려움을 겪는 분들을 위해서 삶의 질 향상에 희망을 드리고, 새로운 바이오의약 산업 개척에 아주 중요한 분야”라며 “이번 심포지엄을 계기로 희귀유전질환 분야의 연구 활성화와 기술 산업화가 촉진돼 궁극적으로 희귀질환 환자의 치료와 지속적인 신약 개발의 토대가 마련되길 기대한다”고 말했다.
심포지엄 첫 날은 희귀질환에 대한 소개부터 최신 연구현황 및 최신 희귀의약품 개발 현황까지 다양하게 다뤄졌다. 첫날 발표된 연자와 주제는 다음과 같다. △Overview of rare disease treatments in Korea(김나경 전 한국희귀・필수의약품센터 원장) △Academic approach of neuromuscular disease(류홍열 연세대 교수) △Optimized new SOD1 aggregation inhibitor extends life span of ALS model mouse and protects spinal neurons, implication for ALS treatment(PRG S&Tech 우태균 책임 연구원) △The Application of L-0tyrosine Polymer for Nanomedicine(Akron 대학 윤양현 교수) △How to Find Disease-Causing Genetic Variations in Rare Disorder?(고려대학교 의과대학 최정민 교수) △The need for new drug in patients with NF2(순청향대 부천병원 이종대 교수) △A clinical trial with nicotinamide riboside for patients with Werner syndrome, EMPOWER(치바 대학교 마사야 코시자카 교수) △Clinical development of TU7710, a fusion protein of activated factor VII with extended half-life(티움바이오 송인영 상무) △Design for Phase 1/2a clinical trials to evaluate safety and efficacy in NF2 patients(PRG S&Tech 박수영 차장) △Exploring HDAC6 inhibitor as an Emerging Therapeutic Strategy for Charcot-Marie-Tooth Disease(종근당 하니나 실장) △ Advanced Therapies Landscape and Role of VCs in it(4BIO Capital Kierna Mudryy 파트너).

심포지엄의 첫 강연을 맡은 김나경 전 한국희귀필수의약품센터 원장은 국내 희귀질환 현황에 대해 발표했다.
2023년 기준 우리나라 정부가 희귀질환으로 지정한 질환의 수는 1165개이며, 희귀질환 관리를 받고 있는 환자는 약 80만명이다.
전 세계적으로 지정된 희귀질환의 수는 1만개가 넘어가며, 희귀질환 환자는 약 3억명으로 추정되고 있다.
최근에는 해마다 다양한 학회, 논문, 저널 등을 통해 약 250개의 질환이 새로운 희귀질환으로 지정되고 있다.
김 전 원장은 희귀질환의 수가 점점 더 빨리 많이 늘어나는 이유는 진단 방법의 발달로 같은 질환이라도 좀 더 세부적을 나눠지기 때문이라고 말했다. 과거에는 위암이면 위암 하나로 분류됐지만, 이제는 변의 여부 등에 따라 좀 더 세부적으로 나뉜다는 것.
김 전 원장은 “전 세계적으로 △급여 △희귀질환에 대한 전문성 △신약 개발 등 희귀질환 환자들이 겪고 있는 어려움을 해소하기 위해 노력하고 있다"고 전했다.
우리나라도 1999년 설립한 ‘한국희귀・필수의약품센터(이하 센터)’를 중심으로 희귀질환 환자를 위한 정책을 진행하고 있다. 센터는 국내에서 유일하게 보험회사를 제외하고 환자를 대신에 급여를 신청할 수 있는 기관이다.
센터는 희귀의약품 국내・외 관련 정보를 수집 및 데이터베이스화하고 있으며, 희귀의약품 관련 정보매체를 개발・보급하고 있다. 또한 위탁제조 등을 통해 희귀의약품 공급을 지원하고, 국내 비유통 의약품을 수입해 필요한 환자에게 공급하고 있다. 아울러 희귀의약품 지정 추천 및 안정적인 공급을 위한 정책 건의도 하고 있다.
김 전 원장은 “현재 우리나라 정책 방향은 희귀질환자에 대한 경제적인 부담을 덜어주고, 신약 개발에 대한 지원을 해주는 방향으로 나아가고 있다”면서 “희귀질환자에 대한 급여 문제는 여전히 정부가 직접 나서서 신경 써줘야 하는 부분”이라고 강조했다.
전세계 희귀의약품 시장은 빠른 속도로 커지고 있다. 2022년 기준 전 세계 제약 시장의 규모는 1조 5000억 달러(약 1940조원)에 달하며 연평균 5%의 성장률을 보이고 있다. 그 중에서도 희귀의약품 시장은 연평균 9%의 성장률을 바탕으로 2012년 전체 제약 시장의 10.5%에서 2020년 16.7%를 거쳐 2024년이면 20.3%에 달할 것으로 전망되고 있다. 이미 제약 선진국 미국에선 희귀의약품이 전체 의약품 시장의 53.7%를 차지하고 있다.
김 전 원장은 "희귀의약품 시장이 커지면서 제약 선진국들은 희귀질환 신약 개발에 큰 관심을 보이고 있다”고 말했다.
미국 FDA는 2020년 53개의 신약을 허가 했는데, 그 중 31개(58%)가 희귀질환 신약이었다. 유럽 EMA도 2016년부터 ‘PRIME 제도’를 도입해 희귀질환 신약 허가에 대한 지원에 나섰다.
제약・바이오 산업을 차세대 먹거리 사업으로 선정한 우리나라도 신약개발에 적극적인 지원을 하고 있다. 최근 희귀・혁신의약품 우선심사를 도입했다. ‘중증・희귀질환 치료제 중 대체 가능한 의약품이 없거나 안전성・유효성이 현저히 개선된 의약품’에 대해 특별한 사정이 없으면 최대 90일 내 결과를 통보해주는 제도다. 현재 우리나라는 2만명 이하의 질환자를 대상으로 한 의약품을 희귀 의약품으로 지정하고 있다. 이는 인구 비율을 적용할 때 미국의 20만명, 일본의 5만명 기준과 유사한 수준이다.
또한 희귀 의약품이 개발되면 대체자가 없는 경우 10년의 재심사 기간을 부여하고 있다. 즉 시장을 10년 동안 독점할 수 있는 권리가 생기는 것이다. 더 나아가 어린이 소아 적응증이 추가될 경우 1년이 연장돼 총 11년의 독점권이 주어진다. 아울러 DMF 자료 면제와 더불어 일반의약품과는 달리 5년 갱신 기간도 없다.

“FDA가 계열 내 최초(First-in-Class), 혁신신약(Novel)을 중심으로 승인(Approval)하는 경향이 강화됐다. 과거보다 신약의 최종 승인은 더 엄격해졌지만, 최신 기술이 접목된 항암제, 희귀유전질환과 같은 미충족 의료 수요가 큰 분야의 신약 승인에는 적극적이다.”
제약산업전략연구원 정윤택 대표의 말이다. 정 대표는 14일 서울 강남구 삼성동 코엑스 B홀에서 열린 '코리아 라이프사이언스 위크 2023' 전시회 내 부대행사로 개최된 '제약·바이오헬스 통계포럼'에 참석, FDA 신약 승인 데이터를 바탕으로 글로벌 신약개발 현황과 전망을 제시했다. 제약산업전략연구원은 제약바이오산업의 비즈니스 모델을 발굴해 국내 기업의 글로벌 진출과 신약개발 역량 강화를 지원하는 연구·컨설팅 기관이다.
코리아 라이프사이언스 위크는 생명과학 및 바이오헬스 산업계의 최신 연구개발 제품과 기술을 한 자리에서 살피고, 수요자와 공급자 간 비즈니스 협력 및 강화를 위해 매년 진행되는 국제 전시회다. 이번 행사는 16일까지 이어진다.
정 대표는 FDA의 신약 승인 검토 활동은 매우 엄격해졌으나, 여전히 승인 가능성은 열려 있다고 강조했다. 정 대표는 “FDA가 한 해 동안 승인하는 신약의 총수는 감소하지 않고 오히려 늘었다”면서 “과거보다 바이오 기반 신약 승인이 최근 많이 증가했다”고 말했다.
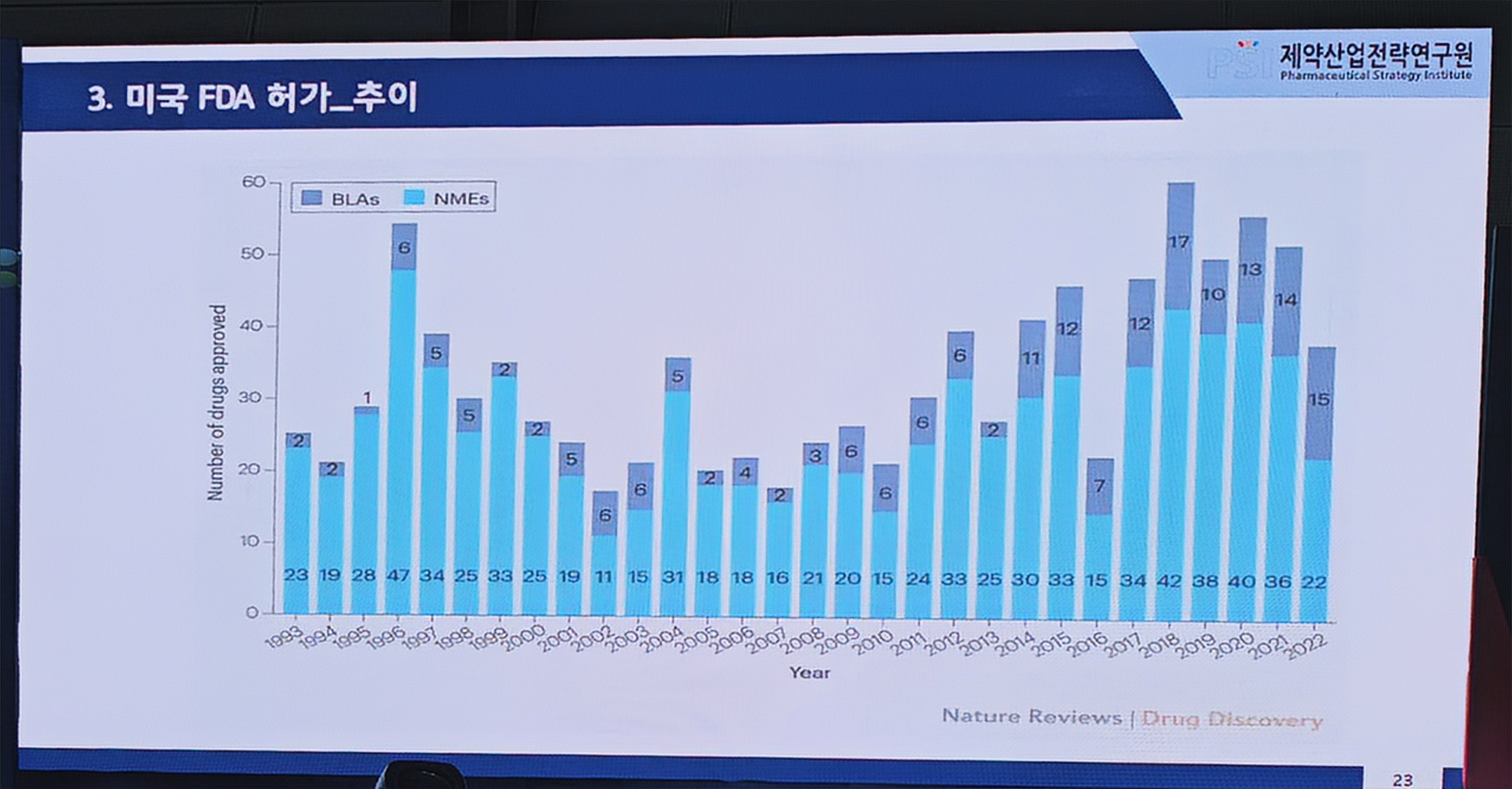
실제 국제 학술지 네이처 리뷰 드럭 디스커버리(Nature Reviews Drug Discovery)에 따르면 FDA는 2014년부터 2022년까지 2016년 한 해만을 제외하고 매년 바이오신약(BLA)을 10건 이상 승인했다. 지난해에도 바이오신약이 15건 승인됐다. 반면 2014년 이전엔 바이오신약은 5건 내외로 승인됐다.
정 대표는 “바이오신약 승인 건수만 증가한 것이 아니라 1세대 바이오신약에서 발전한 새로운 모달리티(Modality, 혁신 치료 기술 총칭) 신약의 승인이 이어지고 있다”면서 “최근 단일항체, 이중항체, ADC(항체약물전합체), 효소(Enzyme), 융합단백질 분야뿐만 아니라 올리고뉴클레오타이드 기반 안티센스(Antisense), siRNA(소간섭RNA) 신약까지도 승인되고 있다”고 전했다.
정 대표는 FDA의 신약 승인 데이터를 △A구간(2006~2015년, 9985건)과 △B구간(2011~2020년, 1만2729건)으로 나눠 분석한 결과, 전반적인 신약 최종 승인 확률은 예전에 비해 최근들어 낮아졌다고 설명했다.
A구간은 임상 1상부터 승인까지 성공률이 9.6%로 분석됐다. 반면 B구간은 7.9%로, A구간보다 약 1.7% 더 낮았다. 심지어 B구간은 1상, 2상, 3상 모든 단계에서 A구간보다 성공률이 낮았다. A구간 단계별 성공률은 1상 63.2%, 2상 30.7%, 3상 58.1%다. B구간은 1상 52%, 2상 28.9%, 4상 57.8%다.
반면 새로운 혁신기술이 접목된 신약의 최종 승인율은 두 자릿수를 넘었다. B구간 기준, CAR-T의 최종 승인율은 17.3%로 전체 신약 승인율 9.6% 대비 두 배 가량 높았다. 이어 siRNA/RNAi 13.5%, 단일항체 12.1%, ADC 10.8%, 유전자치료제 10.0%로 두자릿수 승인율을 기록했다.
정 대표는 “계열 내 최초 신약 승인율이 2021년 54%로, 2017년 33%에서 약 20% 넘게 증가했다”면서 “국내 신약개발 기업도 계열 내 최초, 혁신 기술을 접목한 신약개발을 한다면 높은 FDA 벽을 넘을 수 있다”고 강조했다.

일본 국립성육의료연구센터와 국립암연구센터는 최근 2018~2019년 소아·AYA(Adolescent and Young Adult)세대의 원내암 등록 데어터 집계 결과를 발표했다.
이에 따르면 15세 이상 40세 미만의 AYA 세대는 암환자의 여성비율이 70%를 넘는 것으로 나타났다. 유방암, 자궁경부·자궁암의 비율이 높게 나타났다.
이번 소아·AYA 세대의 암에 특화된 집계·분석은 2019년에 이어 두 번째이다. 데이터는 2018~2019년에 일본 전국의 암진료 제휴 거점 병원 및 소아암 거점 병원 등 원내 암등록 실시 시설에서 새롭게 치료를 개시한 0세~40세 미만의 증례를 대상으로 했다.
데이터에 따르면 15세 미만 소아암에서 암종의 비율은 백혈병 30.4% 뇌종양 23.0%, 림프종 9.8% 순으로 나타났다. 시설별 진료 비중은 소아암을 중점적으로 다루는 소아암 거점병원의 비율이 33.3%였던 반면 암진료 거점병원도 59.0%나 됐다.
한편, AYA세대에서는 여성의 비중이 77%를 차지했고, 연령이 올라갈수록 비중은 커졌다. 여성은 유방암 34.2%, 자궁경부·자궁암 25.4% 갑상선암 14.3% 순으로 많았으며, 남성은 결장직장암 28.1% 갑상선암 14.4% 위암 11.7% 순이었다.
센터는 보고서에 ‘연령에 따라 환자수가 많은 암종이나 성별이 다르다. 앞으로도 계속적인 분석·정보공개가 필요하다’고 지적했다.